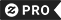Tippe / klicke auf das Bild, um weitere RealViews zu sehenTM
€ 2,15
pro Postkarte
Schwefeleinzelteil der Periodischen Tabelle Postkarte
Menge:
Papiertyp
Signature-Matt
18 pt Stärke / 120 lb Gewicht. Weichweiße, zarte Eierschalenstruktur.
-€ 0,20
Zuschreibung
Über Postcards
Verkauft von
Über dieses Design
Schwefeleinzelteil der Periodischen Tabelle Postkarte
Die с der chemischen Elemente (auch Mendelejews Tabelle, Periodensystem der Elemente oder nur Periodensystem) ist eine tabellarische Darstellung der chemischen Elemente. Obwohl Vorläufer dieser Tabelle existieren, wird ihre Erfindung im Allgemeinen dem russischen Chemiker Dmitri Mendelev im Jahr 1869 zugeschrieben, der die Tabelle dazu diente, wiederkehrende ("periodische") Trends in den Eigenschaften der Elemente zu veranschaulichen. Das Layout der Tabelle wurde verfeinert und mit der Zeit erweitert, da neue Elemente entdeckt wurden und neue theoretische Modelle entwickelt wurden, um das chemische Verhalten zu erklären. Das Periodensystem ist heute innerhalb der akademischen Disziplin der Chemie allgegenwärtig und bietet einen äußerst nützlichen Rahmen zur Klassifizierung, Systematisierung und zum Vergleich aller verschiedenen Formen des chemischen Verhaltens. Die Tabelle hat eine breite Anwendung in der Chemie, Physik, Biologie und Ingenieurwissenschaften gefunden, insbesondere in der Chemieingenieurwissenschaften. Die aktuelle Standardtabelle enthält 117 Elemente, die im Juli 2009 enthalten. 1789 veröffentlichte Antoine Lavoisier eine Liste von 33 chemischen Elementen. Obwohl Lavoisier die Elemente in Gase, Metalle, Nichtmetalle und Erden gruppierte, suchten die Chemiker im folgenden Jahrhundert nach einem präziseren Klassifizierungssystem. 1829 beobachtete Johann Wolfgang Döbereiner, dass viele der Elemente aufgrund ihrer chemischen Eigenschaften in Dreigruppen (Dreier-Gruppen) zusammengefasst werden konnten. Lithium, Natrium und Kalium beispielsweise wurden als weiche, reaktive Metalle zusammengefasst. Döbereiner stellte außerdem fest, dass nach Atomgewicht das zweite Mitglied jeder Triade ungefähr dem Durchschnitt der ersten und dritten Person entsprach. Der deutsche Chemiker Leopold Gmelin arbeitete mit diesem System, und 1843 hatte er zehn Triaden, drei Vierergruppen und eine Gruppe von fünf identifiziert. Jean Baptiste Dumas veröffentlichte 1857 Arbeiten, in denen die Beziehungen zwischen den verschiedenen Metallgruppen beschrieben wurden. Obwohl verschiedene Chemiker in der Lage waren, Beziehungen zwischen kleinen Gruppen von Elementen zu identifizieren, mussten sie erst noch ein System errichten, das sie alle umfasste. Der deutsche Chemiker August Kekulé hatte 1858 festgestellt, dass Kohlenstoff in einem Verhältnis von eins zu vier tendenziell mit anderen Elementen verbunden ist. Methan zum Beispiel hat ein Kohlenstoffatom und vier Wasserstoffatome. Dieses Konzept wurde schließlich als Valency bekannt. 1864 veröffentlichte der deutsche Chemiker Julius Lothar Meyer eine Tabelle mit den 49 bekannten Elementen, die nach Tälern geordnet waren. Die Tabelle zeigte auf, dass Elemente mit ähnlichen Eigenschaften häufig dieselbe Wertigkeit aufweisen. Der englische Chemiker John Newlands veröffentlichte 1864 und 1865 eine Reihe von Arbeiten, in denen er seinen Versuch zur Klassifizierung der Elemente beschrieb: In der Reihenfolge der Erhöhung des Atomgewichts, ähnliche physikalische und chemische Eigenschaften wiederholt sich in Abständen von acht, die er mit den Oktaven der Musik verglichen. Dieses Oktavgesetz wurde jedoch von seinen Zeitgenossen verhöhnt.[8] Das Porträt von Dmitri Mendelejew, dem russischen Chemieprofessor Dmitri Iwanowitsch Mendelejew, und Julius Lothar Meyer veröffentlichten ihre Periodentabellen 1869 bzw. 1870 unabhängig. Beide haben ihre Tische in ähnlicher Weise erstellt: indem die Elemente in einer Zeile oder Spalte in der Reihenfolge des Atomgewichts aufgelistet werden und eine neue Zeile oder Spalte gestartet wird, wenn die Eigenschaften der Elemente zu wiederholen begannen. Der Erfolg von Mendelejews Tisch beruhte auf zwei Entscheidungen: Die erste war, Lücken in der Tabelle verlassen, als das entsprechende Element noch nicht entdeckt worden zu sein schien. Mendelejew war nicht der erste Chemiker, der das tat, aber er ging einen Schritt weiter, indem er die Trends in seinem Periodensystem nutzte, um die Eigenschaften dieser vermissten Elemente wie Gallium und Germanium vorherzusagen. Die zweite Entscheidung bestand darin, gelegentlich die von den Atomgewichten vorgeschlagene Reihenfolge zu ignorieren und benachbarte Elemente wie Kobalt und Nickel zu verändern, um sie besser in chemische Familien einzuteilen. Mit der Entwicklung von Theorien der atomaren Struktur wurde deutlich, dass Mendelev die Elemente unbeabsichtigt in der Reihenfolge der Erhöhung der Atomzahl aufgelistet hatte. Mit der Entwicklung moderner quantenmechanischer Theorien der Elektronenkonfigurationen innerhalb von Atomen wurde deutlich, dass jede Zeile (oder Periode) in der Tabelle mit der Befüllung einer Quantenebene von Elektronen korrespondierte. In Mendelejews ursprünglicher Tabelle war jeder Zeitraum dieselbe Länge. Da größere Atome jedoch mehr Elektron-Subschichten haben, haben moderne Muscheln immer längere Perioden weiter unten am Tisch. In den Jahren, die darauf folgten, als Mendelev sein Periodensystem veröffentlichte, wurden die von ihm links Lücken gefüllt, während die Chemiker mehr chemische Elemente entdeckten. Das letzte natürlich vorkommende Element, das entdeckt wurde, war 1939 Francium (von Mendeleev als eka-caesium bezeichnet). Das Periodensystem ist auch durch die Zugabe von synthetischen und transuranischen Elementen gewachsen. Das erste transuranische Element, das entdeckt werden sollte, war das Neptunium, das durch die Bombardierung von Uran mit Neutronen in einem Cyclotron 1939 gebildet wurde "Periodischer Elementüberblick" Periodische Tabelle der Elemente Dmitri Mendeleev Antoine Lavoisier Chemist Chemistry Physics Labrador Laboratory Experiments Chart Poster August Kekulé Bio physikalischer Analytiker Biochemie Biochemie Biochemische Biologische Biologie Compound Compounds Molecule Molecular Mole Avogadro Formel Symbol "Chemical Symbol" Atom Atomic "Atomic Weight" Proton Neutron Electron Deuterium Tritium Isotope Isomer Molarity Radioactive Nucleus Orbital Spin Quantum Row Zeitraum Actinium Aluminium Argon Argon Arsen Astatine Barium Berkelium Beryllium Bismuth Bohrium Boron Bromine Cadmium Calcium Californium Carbon Cerium Cesium Chrom Cobalt Kupfer Curium Darmstadtium Dubnium Dysprosium Einsteinium Erbium Europium Fermium Fluzium Gadolinium Gallium Gold Hafnium Kalium Helium Holmium Hydrogen Indium Iodine Iridium Krypton Kalziumleder Lithium Lutetium Magnesium Meitnerium Mendelevium Quecksilber Molybdän Neodym Neptunium Nickel Niobium Stickstoff Nobelium Osmium Oxygen Palladium Palladium Platinum Plutonium Polonium Kalium Prasen Eodym Promethium Protactinium Radium Radon Rhenium Rhodium Rubidium Ruthenium Rutherfordium Samarium Scandium Seaborgium Selenium Silicon Silver Sodium Strontium Sulfur Technetium Tellurium Tellurium Terbium Thallium Thorium Thulium Tin Titanium Tungsten Ununbium Ununuum Uranium Vanadium Xenon Ytterbium Yttrium Zink Zirconium
Automatische Übersetzung
Kundenrezensionen
4.8 von 5 Sternen Bewertung6 Bewertungen insgesamt
6 Bewertungen
Bewertungen für ähnliche Produkte
5 von 5 Sternen Bewertung
Von G.16. Februar 2023 • Geprüfter Kauf
Postkarte, Größe: Standard Postkarte, Papier: Signature-Matt, Umschläge: Keine
Bewertungsprogramm bei Zazzle
Sehr schönes Motiv! Passte wunderbar zum Geschenk! Ausgesprochen sehr gut!
4 von 5 Sternen Bewertung
Von Weigant G.12. November 2021 • Geprüfter Kauf
Postkarte, Größe: Standard Postkarte, Papier: Signature-Matt, Umschläge: Keine
Bewertungsprogramm bei Zazzle
Gute Qualität! Schön gemacht! Supet. Tolles Design! Wirklich sehr schön
5 von 5 Sternen Bewertung
Von eva s.21. Februar 2012 • Geprüfter Kauf
Postkarte, Größe: Standard Postkarte, Papier: Signature-Matt, Umschläge: Keine
Bewertungsprogramm bei Zazzle
geschmackvoll, schöne fotokunstkarte, feine Nebelstimmung. Druck und Bearbeitungsmöglichkeiten, Beschriftung etc. sehr gut
zazzle-logo sollte kleiner sein, nimmt zuviel platz weg
Tags
Andere Informationen
Produkt-ID: 239182621914683797
Hergestellt am 10.1.2013, 7:20
G
Zuletzt angesehene Produkte